Actos aparentemente sencillos, como sostenerse de pie o calibrar la presión necesaria para tomar un objeto, requieren en realidad de una sincronización milimétrica entre el cerebro, la médula espinal y los músculos. En personas que presentan una lesión medular incompleta —un tipo de daño donde se preservan ciertas conexiones nerviosas, permitiendo mantener niveles parciales de movimiento y sensibilidad—, estas funciones pueden sufrir alteraciones severas, incluso cuando los pacientes conservan la facultad de desplazarse a pie.
Un estudio reciente ha arrojado luz sobre el origen de esta problemática. Según los hallazgos, el inconveniente principal no reside únicamente en una deficiencia de la fuerza muscular, sino en la forma en que se coordinan las señales nerviosas encargadas de gestionar el movimiento corporal.
Este trabajo investigativo fue liderado por especialistas del KTH Royal Institute of Technology y sus resultados han sido difundidos en la prestigiosa publicación Journal of NeuroEngineering and Rehabilitation, detallando los mecanismos detrás de esta disfunción.
La ruptura del trabajo muscular en equipo
Bajo condiciones de salud óptimas, el sistema nervioso central tiene la tarea de enviar impulsos eléctricos de manera sincronizada hacia los músculos. Esta orquestación garantiza que las fibras musculares operen de forma unísona, produciendo desplazamientos fluidos, exactos y equilibrados.
Para ilustrar este proceso, los expertos sugieren imaginar una orquesta: cada integrante tiene un rol específico, pero todos deben seguir un ritmo común. Esa armonía es la que permite que el cuerpo mantenga el equilibrio o realice ajustes de postura sin que medie un esfuerzo consciente.
No obstante, tras sufrir una lesión medular incompleta, dicha armonía se fractura. Al dejar de recibirse las señales de manera ordenada, los músculos pierden su capacidad de actuar en conjunto. Como consecuencia directa, surgen movimientos inestables y se manifiesta una notable dificultad para modular la fuerza aplicada.
Análisis del sistema nervioso afectado
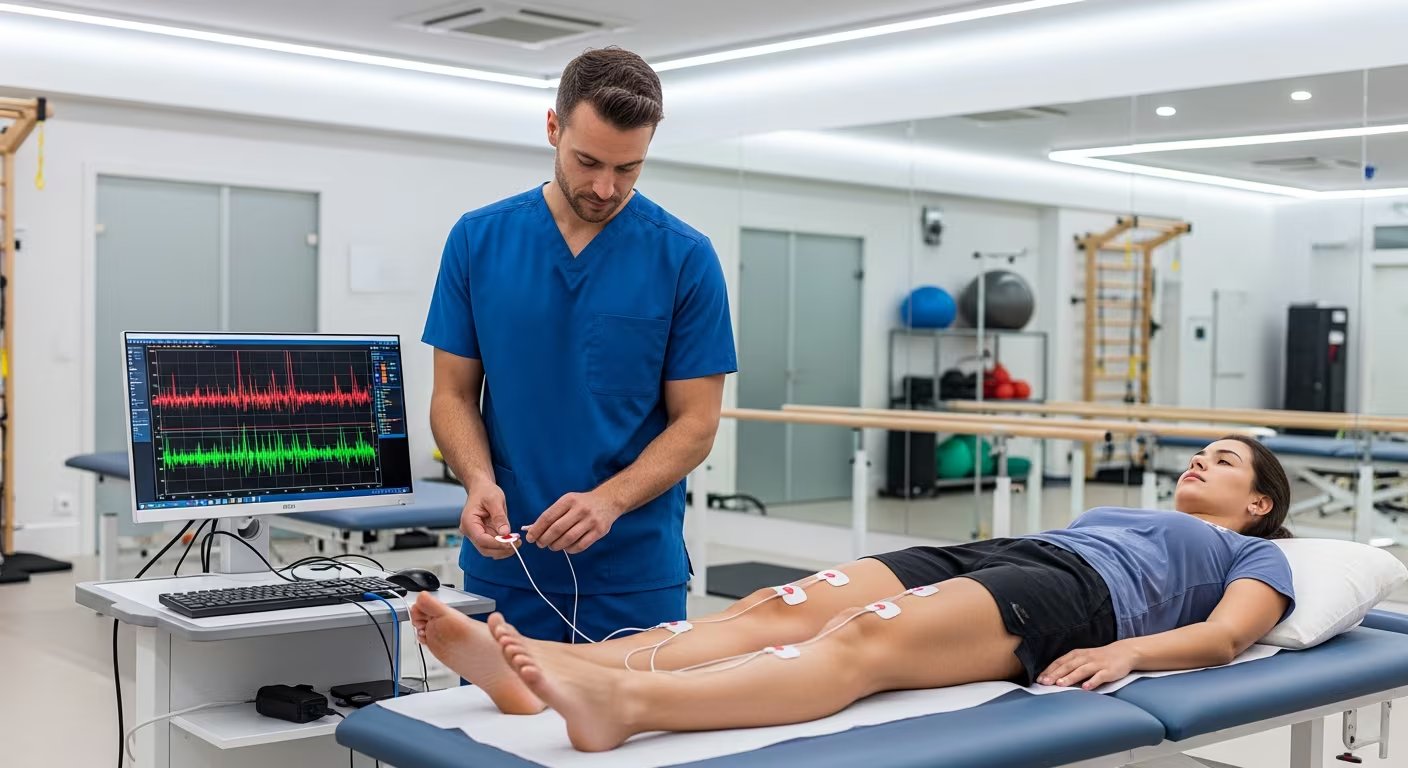
La investigación fue encabezada por la profesora Ruoli Wang y el científico Zhihao Duan. El equipo analizó el comportamiento muscular de 25 voluntarios, un grupo que incluyó a 10 participantes sin lesiones previas para fines comparativos.
Para profundizar en el fenómeno, se emplearon sensores eléctricos de superficie. Esta tecnología de punta permite monitorear la actividad de las denominadas “unidades motoras”, las cuales son agrupaciones constituidas por una neurona y las fibras musculares que esta comanda, siendo el pilar fundamental de cualquier acción motriz.
Los datos obtenidos revelaron que, ante una lesión medular incompleta, la médula espinal ve reducida su capacidad para organizar estas unidades. El impacto es directo sobre la calidad de la ejecución motora, incluso en casos donde la fuerza bruta del individuo parece no haber disminuido significativamente.
Impacto según el grado de esfuerzo aplicado
Uno de los puntos más reveladores del estudio indica que la falta de coordinación varía dependiendo de cuánta intensidad se requiera en la acción. Cuando se solicitó a los voluntarios aplicar apenas el 20% de su fuerza máxima, las órdenes nerviosas se mostraron caóticas. En este nivel, las unidades motoras no lograban activarse simultáneamente, produciendo temblores y complicaciones para sostener posturas fijas.
Por el contrario, al elevar la demanda al 50% de la capacidad de fuerza, el sistema nervioso generaba señales más potentes pero excesivamente rígidas. Lejos de optimizar la coordinación, los músculos actuaban como un solo bloque sólido, lo que impedía realizar los microajustes necesarios para conservar el equilibrio de forma fina.
En términos técnicos, el problema detectado no es la ausencia de señal, sino la pérdida de versatilidad en su regulación. Esto permite entender por qué muchos pacientes con estas lesiones logran caminar, pero enfrentan grandes retos para quedarse quietos o ejecutar gestos de alta precisión.
Mientras que caminar es un proceso más automatizado basado en patrones cíclicos, equilibrarse o graduar la fuerza exige una comunicación constante y refinada entre la musculatura. Si esta red de comunicación falla, incluso las tareas cotidianas más básicas se vuelven un desafío considerable.
Durante el análisis, se identificó un patrón particular en el “impulso nervioso compartido”, que es la señal mediadora de la activación muscular. Este patrón tiene el potencial de convertirse en un biomarcador; es decir, una herramienta de medición objetiva para diagnosticar el estado real del sistema nervioso de un paciente.
El uso de estos indicadores podría revolucionar el diseño de terapias, volviéndolas mucho más personalizadas. El enfoque pasaría de simplemente intentar robustecer los músculos a buscar una mejora sustancial en la sincronización y calidad de los mensajes nerviosos.
Hacia nuevas estrategias de rehabilitación
En la actualidad, gran parte de los procesos de rehabilitación se concentran en la recuperación de la potencia muscular. Sin embargo, los hallazgos de este estudio sugieren que es imperativo integrar el trabajo de coordinación neuromuscular.
Gracias al uso de sensores de alta tecnología, ahora es posible cuantificar cómo se activan las unidades motoras, permitiendo a los terapeutas crear rutinas de ejercicio a medida y aplicar métodos de estimulación focalizada.
Este cambio de paradigma podría elevar los estándares de control motor y estabilidad, factores determinantes para la independencia de los pacientes.
A pesar de los avances, los autores del estudio puntualizan que el tamaño de la muestra es reducido, por lo que los resultados deben ser analizados con prudencia. Asimismo, mencionan la complejidad técnica de identificar la totalidad de las unidades motoras activas en cada prueba.
Aun con estas variables, la investigación constituye un progreso sólido en el entendimiento de la calidad de la señal nerviosa tras un traumatismo medular.
Precisión en la recuperación motriz
Descifrar las fallas de comunicación entre los músculos y el sistema nervioso invita a rediseñar los protocolos de tratamiento actuales. El objetivo no debe ser solo que el paciente se mueva, sino que ese movimiento sea de alta calidad.
El aporte del KTH sienta las bases para este cambio. Al determinar los patrones que generan la inestabilidad, se abre una ruta clara para desarrollar terapias que devuelvan a los pacientes no solo la movilidad, sino también la precisión y el control sobre su propio cuerpo.
Fuente: Fuente