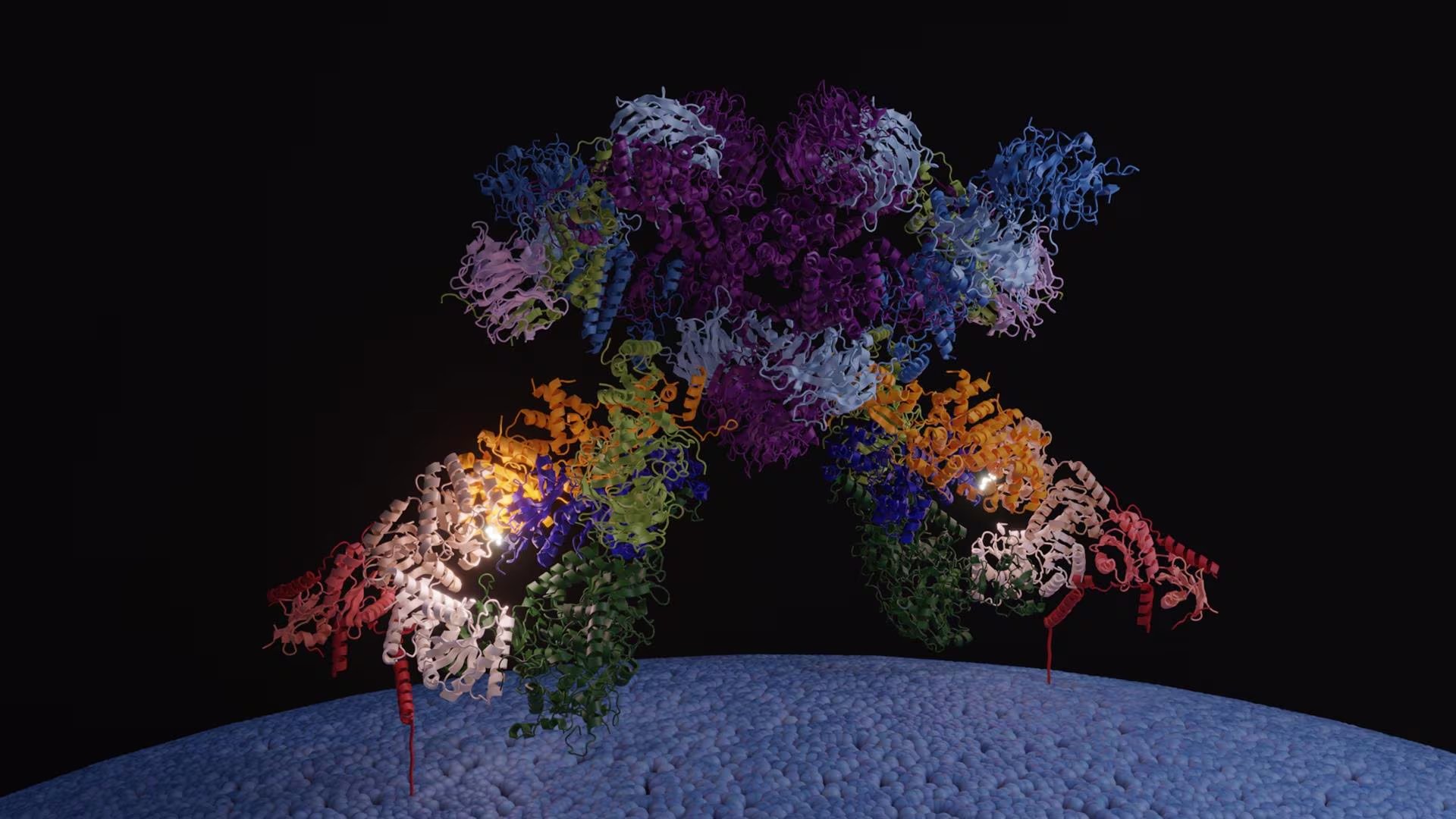
Un avance significativo en la biología molecular ha permitido determinar la estructura del complejo SEA, elemento fundamental en la regulación de la proteína TOR. Este descubrimiento evidencia transformaciones determinantes en la manera en que las unidades celulares captan y procesan los datos sobre la disponibilidad de nutrientes. La investigación, dirigida por Lucas Tafur en el Centro Nacional de Investigaciones Oncológicas (CNIO), proporciona nuevas luces sobre los procesos biológicos que detonan enfermedades como el cáncer, facilitando la creación de tratamientos médicos mucho más específicos.
Las células dependen de diversos sistemas sensoriales para monitorear los nutrientes presentes en su entorno, factores que dictan directamente el ritmo del crecimiento biológico. La proteína TOR —conocida como mTOR en los mamíferos— funciona como un sensor central encargado de evaluar si los recursos son suficientes para la expansión celular o si es necesario activar un modo de ahorro energético. Al respecto, Lucas Tafur señaló:
«Cuando faltan nutrientes, TOR se inhibe y la célula frena el crecimiento, y cuando hay muchos recursos, como aminoácidos o glucosa, pasa al contrario: TOR se activa y promueve el crecimiento celular y la proliferación».
La arquitectura molecular de la proteína TOR
El núcleo de este fenómeno reside en el complejo funcionamiento interno de TOR. Esta proteína no actúa de forma aislada, sino que se integra en dos estructuras moleculares de gran envergadura denominadas TORC1 y TORC2, las cuales están compuestas por múltiples proteínas ensambladas. El control sobre la activación o pausa del crecimiento no es ejecutado directamente por los nutrientes, sino a través de otros complejos proteicos reguladores.
Lucas Tafur, quien lidera el Grupo de Mecanismos Estructurales del Crecimiento Celular en el CNIO, enfatizó que comprender a fondo esta maquinaria es vital para encontrar ventanas de oportunidad en la intervención farmacológica. Según el experto, una aproximación más detallada permitiría reducir los efectos colaterales de los fármacos actuales:
«Un fármaco que interfiera con la actividad total de TOR tiene muchos efectos secundarios. Pero si entendemos en detalle la maquinaria que regula a TOR, podemos encontrar la manera de intervenir más selectivamente».
Modelos biológicos y conservación evolutiva
Para alcanzar estos resultados, el equipo científico utilizó como modelo de estudio la levadura Saccharomyces cerevisiae. El uso de este organismo se justifica por las notables coincidencias estructurales y operativas entre la proteína TOR de la levadura y la versión humana, lo que permite trasladar los hallazgos entre ambas especies. Esta proteína es una pieza clave en la historia de la vida, manteniéndose presente a través de la evolución en organismos tan variados como peces, aves, insectos, primates, humanos e incluso en el reino vegetal.
El origen del nombre de esta proteína se remonta a 1975, tras el hallazgo de la rapamicina en muestras de suelo de la Isla de Pascua. Debido a que la proteína es el blanco de esta molécula, se la denominó TOR (Target of Rapamycin). Aunque la rapamicina ya se utilizaba en la medicina para prevenir el rechazo en trasplantes y combatir tumores por sus capacidades inmunosupresoras, su vínculo directo con TOR no se estableció hasta la década de 1990, posicionándola desde entonces como un pilar de la biomedicina contemporánea.
Tecnología de vanguardia para visualizar átomos
Comprender la organización de estos complejos proteicos representa uno de los mayores desafíos científicos actuales debido a su intrincada forma. Para superar este obstáculo, el equipo de Tafur empleó la técnica de crio-microscopía electrónica. Este método consiste en congelar las muestras biológicas a una temperatura extrema de -196 ℃ utilizando nitrógeno líquido, lo que permite capturar imágenes tridimensionales con una resolución cercana al nivel atómico.
Gracias a esta tecnología, los investigadores lograron descifrar la estructura del complejo SEA, también identificado como GATOR. Este componente es un regulador maestro capaz de centralizar señales metabólicas críticas provenientes de los aminoácidos, la glucosa y el colesterol. A pesar de que su relevancia era conocida, la forma exacta en la que gestionaba dicha información era un misterio hasta ahora.
Un interruptor molecular contra las patologías
Contrario a las hipótesis científicas previas que sugerían que el complejo SEA estaba dividido en dos secciones que se bloqueaban mutuamente, el nuevo estudio demuestra una realidad distinta. La arquitectura de este complejo revela que funciona como una unidad integrada. Tafur aclaró este punto fundamental:
«Vemos que ese concepto no es completamente cierto, no hay una subdivisión dentro del complejo de forma que una parte bloquea a la otra, sino que funciona como un todo».
Asimismo, la investigación arrojó que la alteración de un solo aminoácido es suficiente para desestabilizar por completo el mecanismo de activación de TOR. Este hallazgo es crucial para entender por qué surgen ciertos tumores cuando el sistema falla. El investigador comparó este proceso con un dispositivo electrónico:
«Esta actividad es como un interruptor, que no solamente se necesita —como siempre se ha pensado— para inhibir a TOR, sino que también se necesita para activarlo rápidamente».
En conclusión, el trabajo liderado por Lucas Tafur no solo profundiza en el conocimiento de los engranajes moleculares del cuerpo, sino que establece los cimientos para estrategias terapéuticas disruptivas en enfermedades ligadas al metabolismo. La capacidad de intervenir en puntos milimétricos del sistema promete un futuro donde la medicina pueda modular el crecimiento celular con una precisión sin precedentes.
Fuente: Fuente