La evolución en la identificación temprana del Alzheimer está generando un giro determinante en el manejo clínico de la patología. Actualmente, más de 57 millones de individuos padecen demencia en todo el planeta, y según proyecciones de la Organización Mundial de la Salud (OMS), este volumen de afectados se disparará hasta los 139 millones para el año 2050.
Dado que el Alzheimer constituye entre el 60% y el 70% de los diagnósticos de demencia a escala global, los descubrimientos científicos más recientes ofrecen la esperanza de transformar los métodos y los tiempos de detección. Esto encamina la medicina hacia un modelo de atención personalizada y considerablemente menos invasiva.
Detectar indicios prematuros de la enfermedad mediante una simple extracción sanguínea ha dejado de ser una teoría para convertirse en una realidad tangible. Una investigación profunda difundida en la prestigiosa revista Nature y analizada por el reconocido especialista Eric Topol, destaca cómo los biomarcadores en sangre, con énfasis en la proteína p-tau217 plasmática, se consolidan como un recurso de gran potencial diagnóstico.
El estudio, que contó con el liderazgo de Henrik Zetterberg de la Universidad de Gothenburg y Barbara Bendlin de la Universidad de Wisconsin-Madison, sostiene lo siguiente:
“Múltiples estudios sugieren que el biomarcador más prometedor para el Alzheimer es la p-tau217 plasmática, que captura aspectos de la enfermedad relacionados y proporciona información sobre una respuesta neuronal que predice la neurodegeneración”
.
Bajo el título “Biomarcadores de biofluidos en la enfermedad de Alzheimer y otras demencias neurodegenerativas”, el análisis examina la potencia de estos marcadores para alterar tanto la investigación científica como la práctica médica. Según los especialistas citados en Nature,
“los biomarcadores basados en biofluidos han transformado la investigación y la atención de las enfermedades neurodegenerativas, aportando información sobre las bases moleculares de la enfermedad de Alzheimer y otras demencias neurodegenerativas”
.
El informe resalta que las innovaciones tecnológicas actuales permiten localizar moléculas vinculadas a la neurodegeneración incluso en concentraciones mínimas dentro del torrente sanguíneo. Esto facilita un diagnóstico no invasivo y permite que los pacientes sean derivados a tratamientos de forma más ágil.
Por su parte, la Fundación Pasqual Maragall define estos elementos de la siguiente manera:
“Los biomarcadores son indicadores biológicos que se emplean para medir y analizar procesos corporales normales, condiciones patológicas o respuestas a tratamientos médicos. En la enfermedad de Alzheimer, los biomarcadores juegan un papel esencial al permitir el diagnóstico temprano, incluso antes de la aparición de los primeros síntomas, así como monitorizar el avance de la enfermedad y la evaluación del efecto de posibles tratamientos”
.
Nuevos horizontes en la investigación de biomarcadores
El uso de estas herramientas biológicas plantea un cambio de paradigma: el personal médico podría detectar señales incipientes y observar la evolución del cuadro clínico sin acudir, en primera instancia, a métodos agresivos como la punción lumbar o a complejos estudios de neuroimagen. De este modo, los test de sangre integran la confirmación diagnóstica en la rutina clínica convencional.
La precisión no se limita únicamente a la p-tau217. La combinación de pTau 217 y β-amiloide 1-42 en el plasma ayuda a predecir la existencia de placas cerebrales, una característica distintiva de la enfermedad. No obstante, los expertos advierten que aún deben ajustarse estos métodos debido a la variabilidad biológica individual que puede alterar los resultados.
En un estudio previo de carácter multicéntrico publicado en Jama Neurology, que involucró a más de 2.500 voluntarios en clínicas de Corea del Sur, se analizaron diversas estrategias para mejorar la rentabilidad y precisión del diagnóstico. Se compararon tres enfoques: un punto de corte estándar, umbrales adaptados a subgrupos biológicos y una técnica de doble corte que incluye una franja de incertidumbre diagnóstica.

Los datos revelaron que ajustar los niveles de referencia de la p-tau217 según condiciones específicas como obesidad, anemia o insuficiencia renal, optimiza significativamente la fiabilidad de la prueba. Por ejemplo, en pacientes con patología renal crónica, la personalización del umbral mejoró la precisión de un 0,65 a un 0,83, disminuyendo la necesidad de exámenes extra.
En el grupo con anemia, el ajuste elevó el indicador de 0,80 a 0,86. Por otro lado, para personas con obesidad, la estrategia de “zona gris” o doble corte mostró beneficios en cuanto a costo-efectividad y exactitud, aunque generó entre un 12% y un 39% de resultados que requirieron pruebas de confirmación adicionales en otros subgrupos.
Estos resultados subrayan la relevancia de la medicina de precisión. Según los investigadores de Jama Neurology, adaptar los parámetros a la diversidad biológica de la población fortalece el valor predictivo de los análisis y reduce los gastos operativos en el sistema de salud.
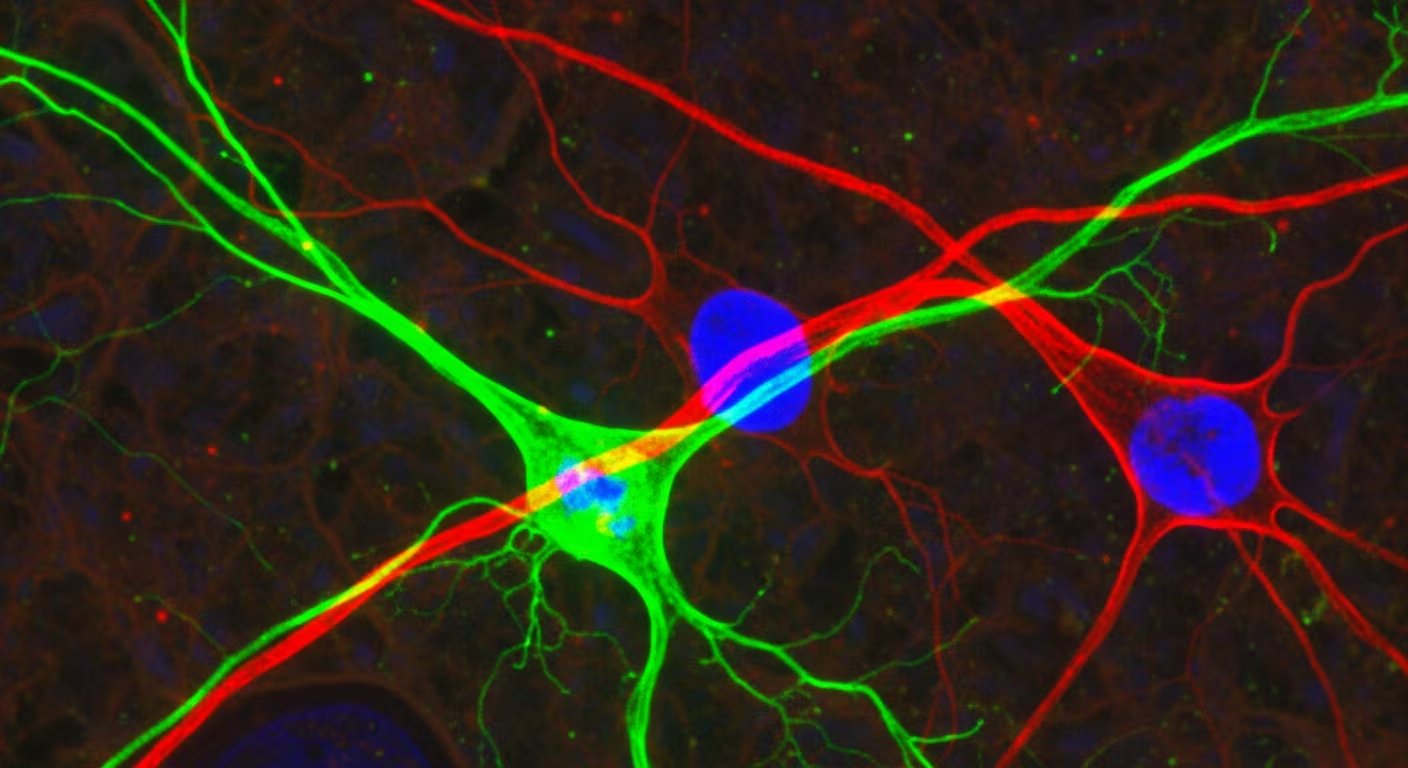
Más allá de la detección, los avances en biomarcadores han impulsado terapias como los anticuerpos monoclonales anti-Aβ. La capacidad de identificar fallos moleculares específicos abre la puerta a nuevas tácticas de prevención y tratamiento a nivel molecular, facilitando la selección de candidatos para ensayos clínicos.
Históricamente, el diagnóstico se basaba en la observación de síntomas cognitivos evidentes. No obstante, el uso de biomarcadores ha revelado una “fase silenciosa” o preclínica, donde los daños en el cerebro se inician mucho antes de que se manifiesten los primeros problemas de memoria o conducta.
Según la revisión en Nature, identificar estos cambios mediante sangre o líquido cefalorraquídeo permite aplicar estrategias preventivas para intentar frenar la progresión hacia la demencia en etapas donde aún no hay signos clínicos pero sí alteraciones detectables.
A estas moléculas se suman las técnicas de imagen como la tomografía por emisión de positrones (PET), que visualiza placas amiloides y la activación glial. El estudio en Nature no solo valida los marcadores actuales, sino que ofrece una guía práctica para su uso diario en los consultorios.

Otro campo de investigación se centra en distinguir formas particulares de la proteína tau, buscando compensar la variabilidad biológica del paciente y perfeccionar el diagnóstico precoz. Estos marcadores permiten además evaluar objetivamente si los tratamientos experimentales están siendo efectivos.
La Fundación Pasqual Maragall aclara que para que estos métodos se usen de forma rutinaria en clínicas, se requieren estudios de cohorte de gran envergadura que ratifiquen su fiabilidad a largo plazo.
Lo que antes se consideraba el inicio de la enfermedad (los síntomas), hoy se entiende como una etapa avanzada. Los biomarcadores permiten detectar señales décadas antes de la aparición de síntomas, lo que resulta vital para intervenir en las fases más tempranas del Alzheimer.

Es importante señalar que poseer una alteración en un biomarcador no garantiza que el paciente desarrollará síntomas clínicos de Alzheimer. Por ello, es imperativo que los resultados se analicen de forma integral junto con la evaluación médica para prevenir diagnósticos erróneos.
La neuroinflamación como factor clave
En una investigación disruptiva liderada por Tomás R. Guilarte en la Florida International University (FIU), se identificó que la TSPO (proteína translocadora de 18 kDa) actúa como un biomarcador temprano de la neuroinflamación ligada al Alzheimer. Este estudio, realizado en modelos animales y muestras humanas, posiciona a la inflamación cerebral como uno de los sucesos más primitivos de la enfermedad.
La TSPO aumenta drásticamente cuando el cerebro experimenta desequilibrios. Mediante un PET, las zonas con inflamación se muestran en tonos rojo anaranjado, permitiendo ver el proceso antes del deterioro cognitivo.

En ratones 5XFAD, el incremento de TSPO fue paralelo a la formación de placas amiloides en el subículo, una región crítica para la memoria. Este fenómeno se detectó apenas a los 1,5 meses de edad en los animales, mucho antes de que mostraran cambios conductuales, los cuales aparecieron a los 7 meses en hembras y 12 meses en machos.
El equipo determinó que este aumento proviene de la microglía activada en contacto con las placas. Estos hallazgos se validaron con tejido cerebral humano post mortem de pacientes con la mutación genética PSEN1-E280A.
Según Tomás R. Guilarte:
“La neuroinflamación es un evento muy temprano en el Alzheimer que influye en su aparición”
. El experto añade que si se utiliza la TSPO para la detección precoz, se podría
“ralentizar la progresión o retrasar los síntomas entre cinco y seis años”
, mejorando la vida de los pacientes.
Aunque los resultados son prometedores, el equipo reconoce limitaciones, como el uso mayoritario de modelos masculinos y de inicio temprano. Por ello, investigadores como Martínez-Pérez ya trabajan con tejidos de casos de inicio tardío para ampliar la validez de estos hallazgos.
La validación clínica total de estos biomarcadores aún requiere procesos rigurosos. No obstante, representan la base de una revolución silenciosa que permite hoy identificar, seguir y tratar el Alzheimer con una precisión sin precedentes.
Fuente: Fuente

