Desde la puesta en marcha del Plan de Abordaje de las Terapias Avanzadas en el año 2019, la infraestructura sanitaria dedicada a los tratamientos CAR-T ha experimentado un crecimiento sostenido en todo el territorio español. Según los datos proporcionados recientemente por el Ministerio de Sanidad, la nación ya cuenta con un total de 40 centros públicos habilitados para la administración de estas innovadoras terapias genéticas contra el cáncer.
La tecnología de las células CAR-T permite la modificación genética de los linfocitos del propio paciente mediante el uso de fármacos específicos, capacitándolos para reconocer y aniquilar de forma selectiva las células tumorales. Este procedimiento está dirigido principalmente a pacientes con cánceres hematológicos —como el linfoma o el mieloma múltiple— que no han mostrado mejoría ante los tratamientos de carácter convencional. Aunque estas terapias recibieron su aprobación inicial en 2017, su integración formal en el sistema de salud español se consolidó tras la validación en 2018 del Plan de Abordaje de las Terapias Avanzadas en el SNS: Medicamentos CAR.
El despliegue de esta red asistencial es notable: actualmente operan 29 centros enfocados en la población adulta y 11 instalaciones especializadas en el área pediátrica. Estas unidades se encuentran distribuidas en 14 de las 17 comunidades autónomas del país. Para el año 2025, se ha confirmado la designación de cinco nuevos centros estratégicos: el Complexo Hospitalario Universitario de Santiago, el de Vigo (Galicia), el Hospital Universitario de Navarra, el Hospital Universitario Miguel Servet (Aragón) y el Hospital Universitari i Politècnic La Fe (Comunidad Valenciana), este último con enfoque en la atención infantil.
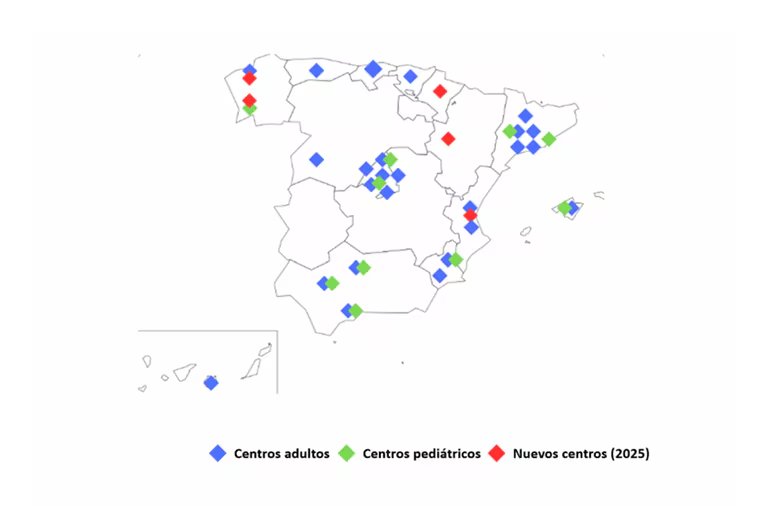
Impacto asistencial: miles de solicitudes tramitadas
El interés por acceder a estas terapias de última generación ha sido masivo desde la creación del circuito nacional de derivación. En los últimos seis años, se han gestionado un total de 2.742 solicitudes de tratamiento provenientes de 184 hospitales de toda España. La eficiencia administrativa ha sido un punto clave, ya que la gran mayoría de estas peticiones son resueltas en un plazo inferior a las 24 horas, alcanzando una tasa de resolución favorable del 93,29%.
En cuanto a la distribución geográfica de la demanda, Cataluña encabeza la lista con 520 peticiones, seguida por la Comunidad de Madrid con 430 y Andalucía con 410. En el extremo opuesto, las regiones con menor número de solicitudes son Cantabria (1), La Rioja (2) y Navarra (3). Respecto al perfil del paciente, los datos revelan que la mayoría son hombres con una edad promedio de entre 62 y 65 años, a excepción de los casos de leucemia linfoblástica aguda B, donde la media de edad desciende drásticamente hasta los 25 años.

Fármacos disponibles y cobertura pública
En la actualidad, el Sistema Nacional de Salud (SNS) financia un total de siete fármacos CAR-T, de los cuales cinco son de origen industrial y dos son de fabricación no industrial. Su aplicación se centra prioritariamente en patologías de origen hematológico de alta gravedad. El linfoma B difuso de células grandes se mantiene como la afección más tratada con esta tecnología, seguida de la leucemia linfoblástica aguda B. Asimismo, el Ministerio de Sanidad ha detectado un repunte en las peticiones para tratar el mieloma múltiple, lo que refleja la “reciente incorporación de nuevas indicaciones clínicas” en el catálogo público.
Dentro del arsenal terapéutico disponible, los medicamentos axicabtagén ciloleucel (Yescarta) y tisagenlecleucel (Kymriah) son los que presentan una mayor demanda. Ambos son de naturaleza industrial y cuentan con un esquema de financiación restringida, lo que implica que el sistema público los cubre exclusivamente para tumores y situaciones clínicas muy delimitadas. Por ejemplo, el Yescarta se autoriza para el linfoma B difuso de células grandes en tercera línea, el linfoma B de alto grado en segunda línea, el linfoma B primario mediastínico en tercera línea y el linfoma folicular en cuarta línea de tratamiento.
Por otra parte, el Kymriah cuenta con respaldo financiero para intervenciones de tercera línea en casos de linfoma B difuso de células grandes, además de estar indicado para pacientes con leucemia linfoblástica aguda que superen los 25 años de edad.
Fuente: Fuente

