Los genomas de los fagos —denominados así a los virus que tienen la capacidad de infectar bacterias— se encuentran integrados en su gran mayoría por lo que los científicos llaman «materia oscura». Se trata de una serie de genes que dan lugar a proteínas cuyas utilidades biológicas todavía permanecen en el misterio. Hace menos de un lustro, un equipo de especialistas bajo el mando del profesor Rotem Sorek, perteneciente al Instituto Weizmann de Ciencias, logró identificar una nueva clase de proteína dentro de este enigma viral, bautizándola con el nombre de “esponja”.
Estas estructuras, conocidas como proteínas de esponja virales, poseen una naturaleza porosa y están diseñadas específicamente para capturar moléculas en cavidades internas de gran profundidad, emulando la capacidad de absorción de una esponja común con el agua. Sin embargo, para los fagos, esta esponja funciona como un arma estratégica: su función es interceptar las moléculas de comunicación que son fundamentales para la respuesta inmunitaria de la bacteria. Al quedar atrapadas estas señales, el fago logra tomar las riendas de la célula bacteriana, multiplicándose en su interior sin enfrentar resistencia alguna.
La inteligencia artificial al servicio de la biología
Hasta hace poco, se habían descubierto muy pocas proteínas de esponja debido a que sus secuencias genéticas son extremadamente variadas, lo que complicaba enormemente su localización con métodos tradicionales. No obstante, empleando una metodología de investigación disruptiva que entrelaza la inteligencia artificial con la biología de experimentación, el laboratorio de Sorek ha conseguido hallar nuevas familias de estas proteínas capaces de boicotear la comunicación inmune bacteriana.

Los hallazgos, publicados en la prestigiosa revista Science, exponen detalladamente cómo los agentes virales consiguen silenciar las alarmas biológicas del sistema inmunológico. El estudio subraya la relevancia de este sabotaje comunicativo en el conflicto evolutivo que mantienen virus y bacterias desde hace milenios.
Durante esta nueva fase de investigación, los expertos analizaron las configuraciones de las proteínas de esponja que se conocían previamente, detectando un patrón de diseño arquitectónico que se repite y que sirve como guía para nuevas detecciones.
“Todas son pequeñas, están compuestas por varias subunidades idénticas y contienen cavidades profundas”, explica Sorek. “Estas cavidades poseen una carga eléctrica positiva, lo que les permite absorber moléculas de alarma inmunitaria, que normalmente tienen carga negativa”.
En este proceso, el factor humano también jugó un rol determinante. “La aguda observación de un estudiante nos ayudó a identificar una nueva familia de proteínas de esponja, un recordatorio de que la perspicacia humana sigue siendo importante en la era de la IA.”

Si bien anteriormente este tipo de hallazgos carecían de una aplicación práctica inmediata, la integración de la inteligencia artificial ha modificado este panorama de forma radical.
“Nos dimos cuenta de que, con herramientas avanzadas de IA como AlphaFold de Google, podíamos analizar una enorme cantidad de proteínas y buscar aquellas con cavidades cargadas positivamente capaces de atrapar moléculas inmunitarias”, explica el Dr. Nitzan Tal, quien dirigió el nuevo estudio en el laboratorio de Sorek. “Esto nos permitió descubrir nuevas funciones de las proteínas de los fagos basándonos únicamente en su estructura”.
Un análisis a gran escala
El equipo de científicos procesó una base de datos masiva de 32 millones de genes que codifican proteínas de fagos, extraídos de un total de 2 millones de genomas virales. Para predecir las estructuras en tres dimensiones, recurrieron a la tecnología de AlphaFold. “Encontramos más de 120 candidatos cuyas estructuras coincidían con nuestros criterios y pasamos a las pruebas experimentales”, detalló el doctor Tal.
Tras la fase de selección, se procedió a testear la efectividad de cada candidato frente a cinco tipos de sistemas inmunitarios en bacterias. Para ello, se utilizó una técnica innovadora creada por el investigador Jeremy Garb en el mismo laboratorio de Sorek. Este sistema permitió que el equipo ejecutara todas las comprobaciones de manera simultánea, evitando la necesidad de realizar cientos de ensayos individuales por separado.

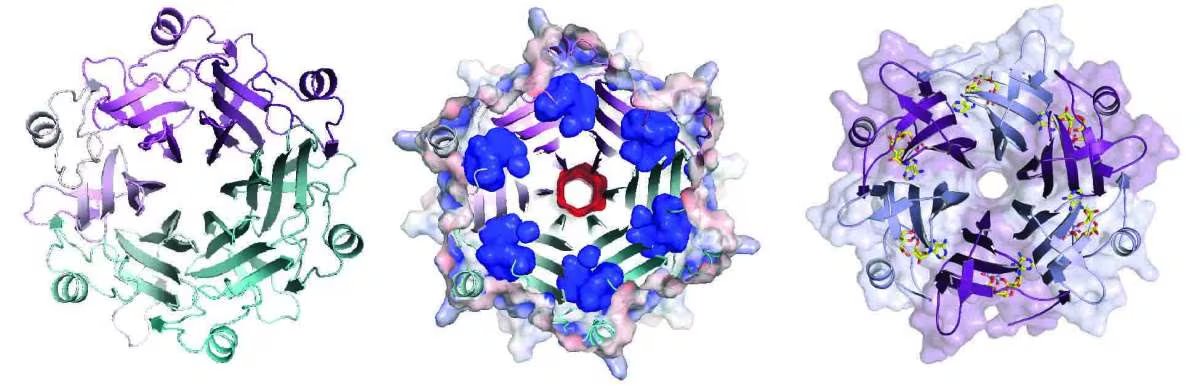
Los resultados de estos experimentos sacaron a la luz una familia inédita de proteínas esponja que ha sido denominada Lockin. Gracias al modelo de inteligencia artificial, se pudo predecir que estas proteínas se estructuran con seis subunidades iguales que forman un círculo, similar a los pétalos que componen una flor. En una acción conjunta con el profesor Philip J. Kranzusch del Instituto de Cáncer Dana-Farber de Boston, se logró determinar la estructura de un integrante de esta familia mediante cristalografía de rayos X, validando la predicción de la IA y entendiendo exactamente cómo se captura la señal de alarma.
“La enorme base de datos de proteínas virales que analizamos se obtuvo principalmente mediante la secuenciación de muestras de ADN ambiental que incluyen una gran mezcla de fagos”, comenta Sorek. Esto permitió que se encontraran las proteínas Lockin en cientos de virus que jamás habían sido aislados dentro de un laboratorio.
Nuevas familias identificadas
Más allá de la inteligencia artificial, el laboratorio aplicó otras tácticas creativas. Romi Hadary, otra investigadora del equipo, notó que los genes encargados de codificar proteínas esponja conocidas tienden a aparecer fusionados dentro de los genomas de los fagos.
Este hallazgo facilitó la identificación de otra familia denominada Sequestina, detectada precisamente porque sus genes se presentan fusionados con los de esponjas ya identificadas anteriormente. “Esto demuestra que, incluso en la era de la inteligencia artificial, las agudas observaciones de los científicos humanos siguen siendo de gran valor”, puntualizó Sorek.
El estudio también presentó a la familia Acb5, la cual generó dudas iniciales en los investigadores.
“Estas proteínas eran muy similares a las proteínas de las esponjas, pero descubrimos que no solo atrapan moléculas de alarma, sino que también las cortan”, explica Tal. “Esto fue sorprendente porque no presentaban las características estructurales típicas de las herramientas de corte molecular. Este descubrimiento demuestra cómo el análisis estructural sistemático puede refutar supuestos científicos previos”.
Hacia nuevas fronteras terapéuticas
Las familias proteicas halladas en esta investigación están presentes en miles de fagos distribuidos en la naturaleza. Se descubrió, además, que un único virus puede estar equipado con un arsenal variado de enzimas y proteínas destinadas a neutralizar al sistema inmune bacteriano, lo que les otorga una ventaja competitiva en su lucha biológica.
“Aún se desconoce si los virus que infectan a plantas, animales y humanos también utilizan proteínas esponja, pero el enfoque computacional y experimental que hemos desarrollado permite comprobarlo”, señaló el profesor Sorek. De confirmarse esta posibilidad, estas proteínas podrían ser el blanco perfecto para la creación de nuevas terapias antivirales. El método utilizado no depende de conocimientos previos ni de cultivos de laboratorio, convirtiéndose en una herramienta sumamente potente para explorar el sistema inmunitario.
Cabe destacar que, actualmente, se desconoce la función de aproximadamente el 70 por ciento de los genes de los fagos, lo que deja un amplio margen para futuras investigaciones.
En este estudio colaboraron figuras como el Dr. Ilya Osterman, el Dr. Gil Amitai, Erez Yirmiya, la Dra. Nathalie Béchon, la Dra. Dina Hochhauser y Barak Madhala, todos del Departamento de Genética Molecular de Weizmann; además de Renee B. Chang y Miguel López Rivera del Instituto Oncológico Dana-Farber; Roy Jacobson, el Dr. Moshe Goldsmith y la Dra. Tanita Wein, también del Instituto Weizmann.
Fuente: Fuente