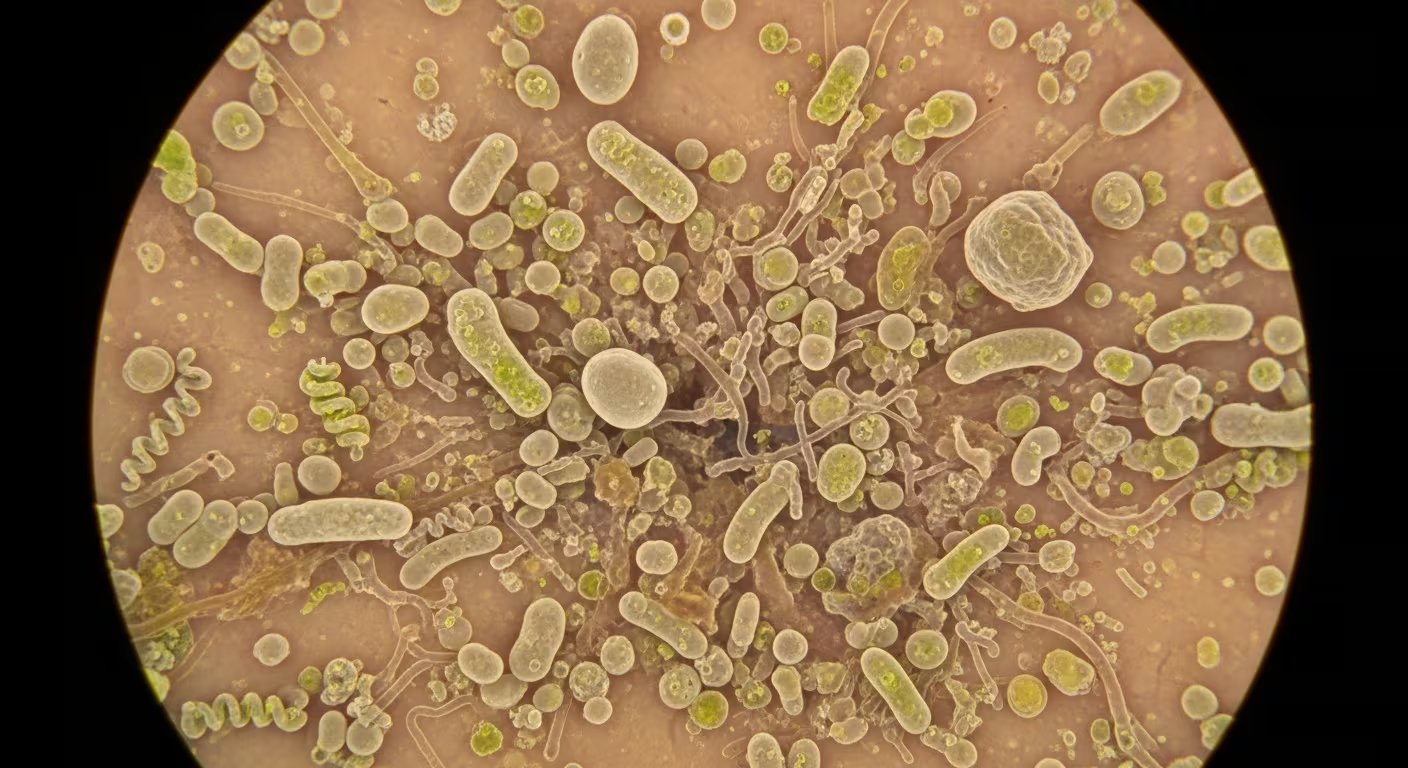
La aparición y el avance de diversas superbacterias resistentes, entre las que destaca el hongo Candida auris, han generado una profunda preocupación en los centros hospitalarios de Nueva York y Nueva Jersey. Esta situación ha forzado a las autoridades a intensificar de manera urgente los protocolos sanitarios para mitigar brotes de infecciones cuya complejidad terapéutica es elevada.
El Candida auris es un hongo de tipo patógeno que se detectó por primera ocasión en Japón durante el año 2009. Posteriormente, en 2016, el microorganismo consolidó su presencia en el territorio de los Estados Unidos. Según los informes de los Centros para el Control y la Prevención de Enfermedades (CDC), su propagación a nivel global se ha visto favorecida por la presión selectiva que genera el uso masivo de antibióticos y antimicóticos en las instituciones de salud.
De acuerdo con reportes del New York Post correspondientes a la primera mitad de 2024, las zonas de Nueva York y Nueva Jersey agruparon cerca del 20% de la totalidad de casos registrados en la nación. Las cifras oficiales detallan la existencia de 623 casos clínicos y un total de 849 portadores asintomáticos. Estos datos ratifican la alta capacidad de este hongo para adaptarse a diversos entornos y permanecer en las superficies de los hospitales, incluso después de haberse ejecutado protocolos de limpieza y desinfección.
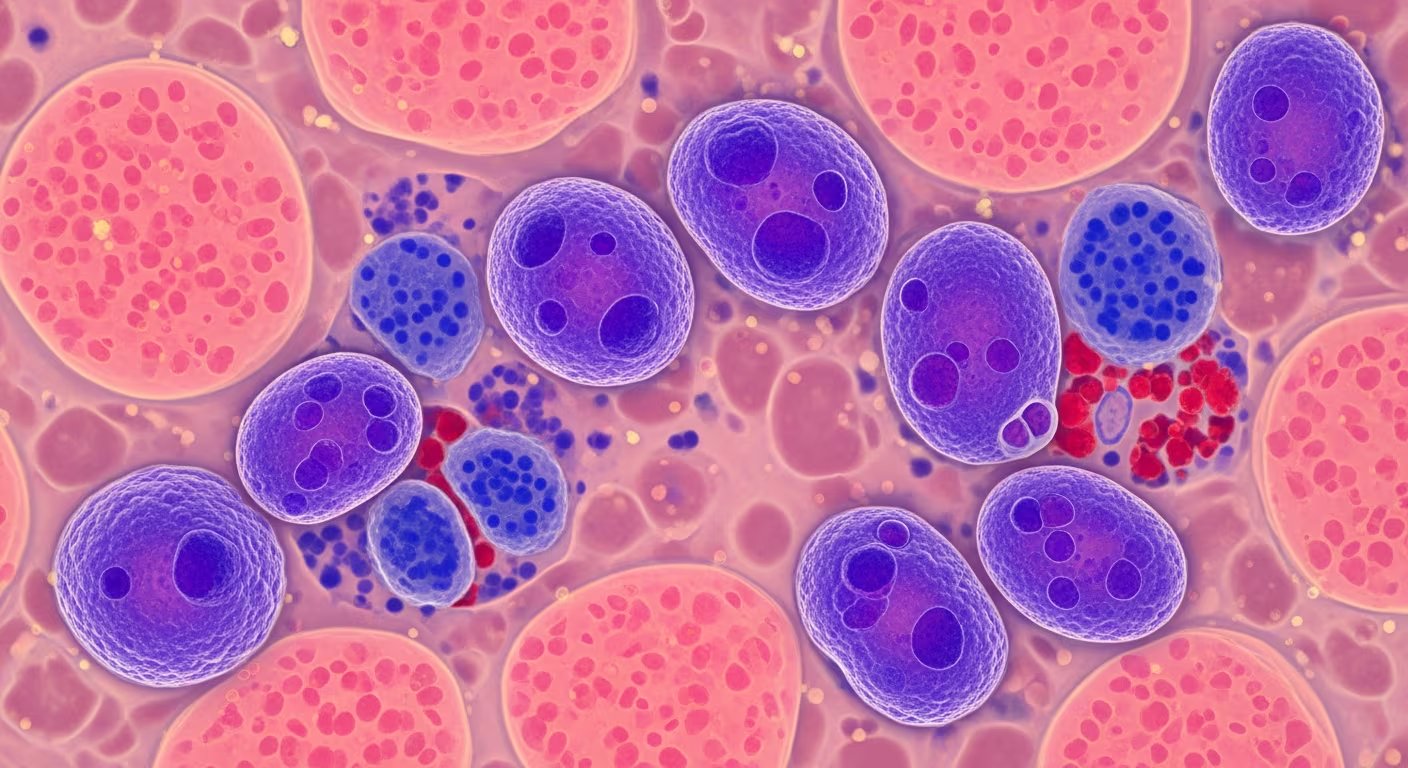
La resistencia que caracteriza al Candida auris se origina principalmente por el empleo sin control de fármacos antimicóticos y antibióticos, lo cual permite la supervivencia de cepas que no responden a los tratamientos médicos habituales.
Mecanismos de resistencia y mutación genética
A nivel biológico, este mecanismo defensivo se vincula con mutaciones específicas en genes clave. Entre ellos se encuentra el ERG11, que es el encargado de sintetizar la enzima lanosterol 14α-desmetilasa, y el gen TAC1b. Estas alteraciones provocan que el hongo sea resistente a los azoles, una familia de antifúngicos esenciales. Investigaciones validadas por el National Institutes of Health (NIH) y publicaciones en Microbiological and Molecular Biology Reviews, así como en Frontiers in Cellular and Infection Microbiology, señalan que más del 80% de las muestras clínicas presentan resistencia al fluconazol. Incluso, se han detectado variantes multirresistentes que pueden eludir hasta cuatro tipos diferentes de fármacos.

La evolución de esta resistencia no solo responde a mutaciones genéticas, sino también a la presión selectiva de los medicamentos y a una transmisión sumamente eficaz dentro de las instalaciones médicas. El uso inapropiado de antimicrobianos, la tendencia a la automedicación y la prescripción errónea de antibióticos para cuadros virales son factores que impulsan el desarrollo de estas variantes. Estudios liderados por el Sun Yat-Sen Memorial Hospital de China y el NIH han identificado mutaciones en ERG11 (específicamente Y132F, K143R y F126L) que otorgan resistencia a los azoles, además de cambios en el gen FKS1 relacionados con la ineficacia de las equinocandinas.
El contagio se produce generalmente a través de superficies u objetos contaminados, equipos médicos o el contacto directo entre individuos. Debido a su capacidad para sobrevivir en el entorno hospitalario por tiempos prolongados y su resistencia a ciertos desinfectantes de uso común, el control de los brotes representa un desafío mayúsculo para la vigilancia epidemiológica. Los pacientes con sistemas inmunológicos comprometidos, aquellos en estado crítico o quienes reciben tratamientos prolongados con antibióticos son los más vulnerables. Al respecto, los CDC advierten sobre la gravedad de la situación:
“Más de uno de cada tres pacientes con infección invasiva por Candida auris fallece”
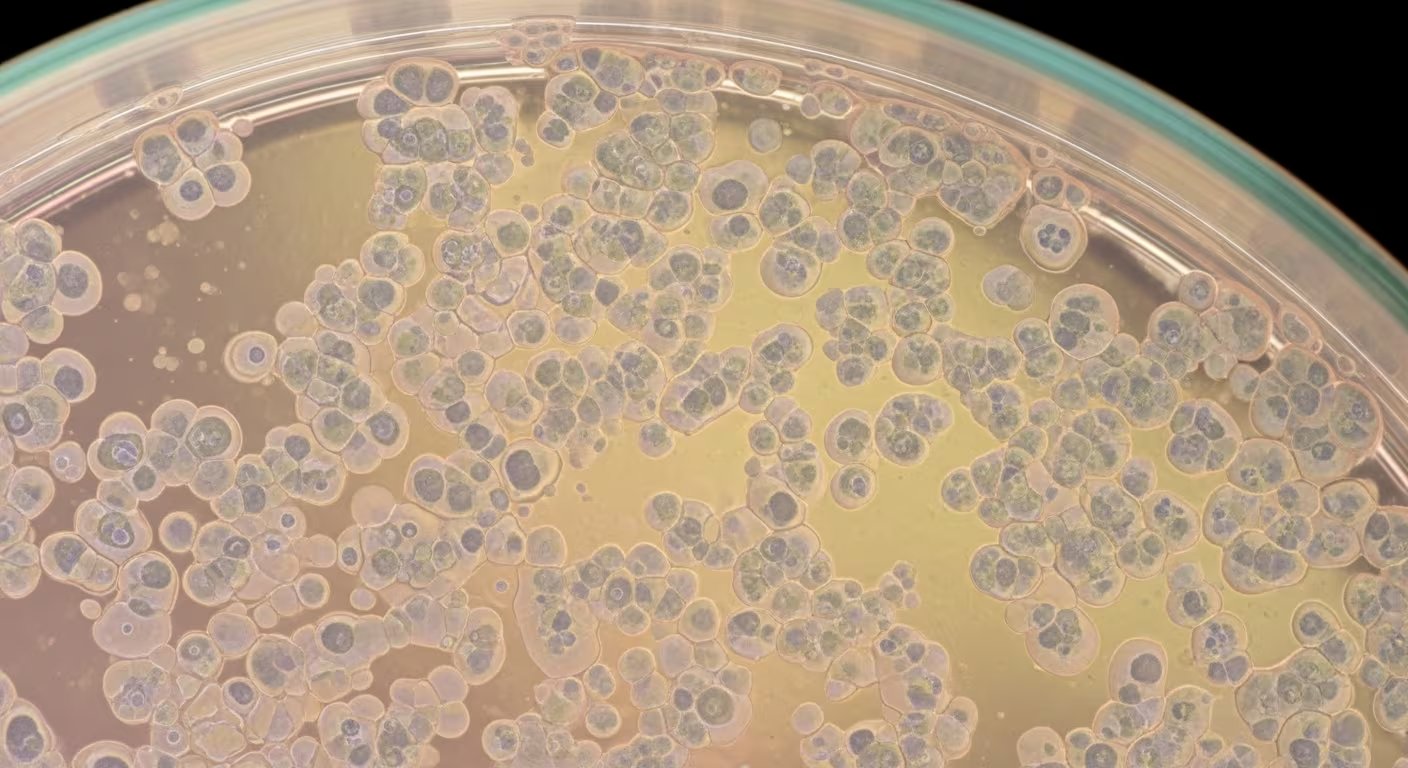
Diagnóstico preciso y nuevas rutas de tratamiento
Uno de los mayores obstáculos es el diagnóstico acertado. La microbióloga clínica de la Clínica Mayo, Nancy Wengenack, sostiene que la identificación de este hongo requiere tecnologías avanzadas como la espectrometría de masas MALDI-TOF o pruebas de PCR dirigida, puesto que mediante la microscopía tradicional no se logran distinguir sus rasgos particulares. Un retraso en el diagnóstico conlleva un inicio tardío del tratamiento, facilitando que la infección se extienda.
Aunque el protocolo estándar se apoya en el uso de equinocandinas, la resistencia creciente ha forzado a los médicos a buscar alternativas como la anfotericina B liposomal o la combinación de diversos fármacos. Actualmente, se investigan nuevas opciones como el fosmanogepix, la rezafungina y el ibrexafungerp. Datos publicados en Frontiers in Cellular and Infection Microbiology revelan que el fosmanogepix alcanzó una tasa de supervivencia del 85% tras 30 días en pacientes con candidemia, sin presentar efectos secundarios de gravedad.
Paralelamente, la ciencia explora terapias con anticuerpos monoclonales dirigidos a proteínas como Hsp90 y Hyr1p, nanoterapias y el uso de antifúngicos de origen natural, los cuales han reducido la mortalidad en pruebas con modelos animales. En cuanto a la prevención, los pilares fundamentales siguen siendo:
- Vigilancia activa y constante en entornos de riesgo.
- Aislamiento estricto de pacientes portadores.
- Higiene de manos rigurosa por parte del personal y visitantes.
- Desinfección de áreas con agentes potentes como la lejía.
Finalmente, los especialistas recalcan que la lucha contra el Candida auris exige un enfoque multidisciplinario que combine el uso responsable de medicamentos, innovación en la investigación farmacéutica y una normativa sólida que regule la práctica médica para evitar futuras amenazas sanitarias.
Fuente: Fuente