De acuerdo con las advertencias de la Organización Mundial de la Salud (OMS), el envejecimiento de la población se ha consolidado como uno de los retos más críticos del presente siglo. Las estadísticas de la entidad señalan que la esperanza de vida global ya supera los 73 años, y las proyecciones para el año 2050 indican que más de 2.100 millones de individuos habrán cruzado el umbral de los 60 años.
Este panorama demográfico trae consigo un incremento en las enfermedades neurodegenerativas, patologías que actualmente afectan a 57 millones de personas a escala mundial y cuya prevalencia, según la OMS, podría duplicarse cada dos décadas. Ante este escenario, un consorcio internacional de expertos bajo la coordinación del Instituto Salk, referente en neurobiología, ha presentado el primer atlas epigenético unicelular enfocado en el envejecimiento del cerebro.
Esta investigación, que ha sido difundida a través de la revista científica Cell, se llevó a cabo utilizando modelos animales. El equipo desarrolló una innovadora herramienta tecnológica que facilita la observación detallada de cómo el paso del tiempo activa ciertos segmentos del ADN que solían estar inactivos dentro de las células cerebrales, permitiendo una precisión sin precedentes en este campo.
En términos prácticos, este descubrimiento ofrece la posibilidad de localizar qué regiones y qué tipos celulares específicos del cerebro sufren un deterioro prematuro. Este avance es fundamental para lograr diagnósticos más tempranos y para la creación de terapias personalizadas orientadas a mitigar o posponer los efectos de condiciones como el Alzheimer.
Respecto a la relevancia de este trabajo, Joseph R. Ecker, quien fungió como director del estudio, manifestó:
“Los cambios cerebrales relacionados con la edad, particularmente en regiones críticas para la atención, la memoria, la emoción y las funciones motoras, afectan gravemente la calidad de vida”.
Por tal motivo, el experto explicó que este atlas es el resultado de un procesamiento masivo de datos de más de un millón de células pertenecientes a cerebros de ratones.
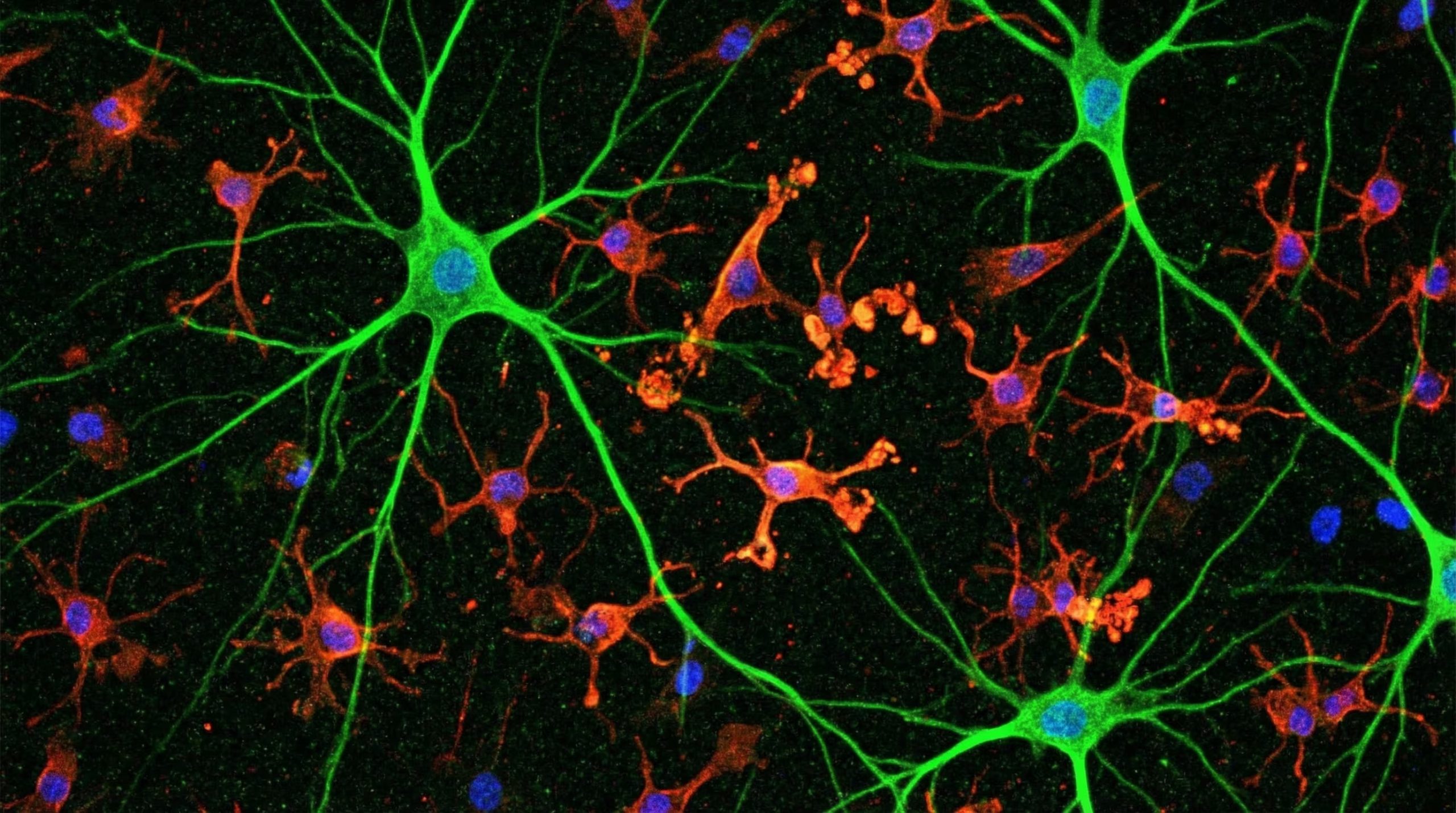
Los investigadores lograron mapear las variaciones epigenéticas —aquellas marcas químicas que determinan la activación o desactivación genética— en 36 clases distintas de células repartidas en ocho áreas del cerebro. El estudio integra metodologías de metilación, transcriptómica espacial y análisis tridimensional del genoma, lo que permite visualizar cómo estas alteraciones moleculares fluctúan según la edad del sujeto, el tipo de célula y su ubicación anatómica.
Descubrimientos del primer atlas epigenético cerebral
Uno de los puntos más destacados de la investigación es la reactivación de los denominados elementos transponibles, conocidos popularmente como “genes saltarines”. Estos fragmentos representan casi la mitad del genoma de los seres humanos y usualmente se mantienen bloqueados mediante la metilación, un proceso químico que actúa como un precinto de seguridad.

Los resultados del atlas confirman que, conforme el organismo envejece, estos precintos químicos pierden fuerza, permitiendo que los “genes saltarines” se activen. Esta liberación provoca una inestabilidad genómica y procesos inflamatorios crónicos, elementos que son determinantes en la degradación celular observada en enfermedades como el Alzheimer y la esclerosis lateral amiotrófica (ELA).
Para entenderlo mejor, la metilación actúa como una cerradura que mantiene clausuradas partes específicas del código genético para prevenir anomalías. Al debilitarse con los años, estos segmentos de ADN adquieren movilidad dentro del genoma, rompiendo el equilibrio interno de las células.
El equipo científico detectó puntos críticos de pérdida de metilación, principalmente en vestigios retrovirales antiguos, con comportamientos que varían drásticamente según la zona del cerebro. Este fenómeno de pérdida de “silenciadores” moleculares no ocurre de forma equitativa, pues existen regiones y células que presentan una mayor fragilidad ante este proceso.

Esta capacidad de análisis detallado es posible gracias a la resolución espacial y unicelular del atlas, el cual se encuentra disponible en infraestructuras como Amazon Web Services y el Gene Expression Omnibus (GEO). Al ser un repositorio de datos biomédicos de libre acceso, permite que científicos de todo el planeta contrasten sus hallazgos con esta base de datos global.
Gracias a esta base informativa, se pudo corroborar que el cerebro no envejece de manera uniforme. Tanto las neuronas como las células no neuronales —específicamente la glía, encargada de la protección, nutrición y soporte neuronal, además de regular el sistema inmune cerebral— muestran tiempos y niveles de vulnerabilidad epigenética distintos.
Se observó que las alteraciones por la edad son más agudas en las células no neuronales. Un ejemplo de esto es que las células gliales ubicadas en la zona posterior del cerebro presentan niveles superiores de inflamación y desajustes genéticos en comparación con las que se encuentran en la región frontal.
Bajo una metáfora botánica, si el cerebro fuera un jardín, la glía representaría el suelo y el entorno que, aunque no es la flor principal como las neuronas, resulta indispensable para el ecosistema. Esta estructura es la más sensible al paso del tiempo y su deterioro depende directamente del “terreno” anatómico donde se ubique.

Adicionalmente, el estudio señaló el fortalecimiento de los límites de los dominios de asociación topológica (TAD) como un indicador preciso del envejecimiento. Estos dominios son segmentos de ADN que interactúan en un espacio tridimensional y su ordenamiento está ligado a proteínas como la CTCF. En esencia, cuando estos límites se alteran, la arquitectura del genoma cambia, perjudicando la comunicación entre distintas áreas celulares.
Este fenómeno puede compararse con un edificio donde las paredes internas se modifican con los años, alterando los pasillos y el flujo de personas, lo que finalmente trastoca la funcionalidad y la comunicación dentro de la construcción.
La alta fidelidad del atlas se obtuvo mediante la caracterización de casi 900.000 células con técnicas de transcriptómica y más de 200.000 células a través de ensayos de metilación. Esto permitió rastrear cómo el tiempo impacta de forma dispar incluso a células idénticas, dependiendo de su posición; así, una célula puede parecer joven en una región pero mostrar signos de vejez avanzada en otra.
Modelos de predicción y el futuro de la medicina personalizada
La publicación de este atlas no solo democratiza el acceso a la ciencia, sino que impulsa la creación de modelos computacionales avanzados. Los expertos del Instituto Salk han diseñado sistemas de aprendizaje profundo (deep learning) que pueden predecir variaciones en la expresión de los genes según la edad del paciente.
Actualmente, este atlas se suma a otros recursos globales de acceso abierto, como el Atlas Cerebral de Allen y el Atlas de Células Cerebrales de la Enfermedad de Alzheimer de Seattle. Esta red de información en la nube facilita la cooperación internacional y elimina obstáculos técnicos para laboratorios con menos recursos.
Los resultados subrayan que mantener una vejez digna depende estrechamente de la salud del cerebro y de la capacidad de respuesta de los sistemas de salud. Según el Instituto Salk, comprender estos mecanismos moleculares es el primer paso para desarrollar intervenciones preventivas y tratamientos a medida.
Finalmente, los datos recolectados abren la puerta a identificar marcas químicas que podrían ser blancos terapéuticos. Existe la posibilidad teórica de “reiniciar” el epigenoma para devolverle su funcionalidad a las neuronas antes de que los daños sean permanentes. Al intentar restablecer los “candados” químicos sobre el ADN inestable, se podría detener el avance del deterioro cognitivo, aunque los investigadores aclaran que todavía queda mucho camino por recorrer en la experimentación clínica.
Fuente: Fuente