Un consorcio internacional de científicos ha logrado desentrañar con mayor detalle el mecanismo mediante el cual el cerebro humano calibra, segundo tras segundo, el flujo de sangre que recibe para su funcionamiento. Esta investigación de vanguardia fue liderada por el catedrático David Kleinfeld y el especialista posdoctoral Ji Xiang, ambos pertenecientes a la Universidad de California- San Diego.
Los hallazgos han sido publicados en la prestigiosa revista científica Proceedings of the National Academy of Sciences, ofreciendo una visión integral sobre cómo la compleja trama de vasos sanguíneos cerebrales logra redistribuir la circulación con una exactitud que, hasta ahora, no se comprendía plenamente.
El desafío energético del órgano pensante
Aunque el cerebro apenas representa el 2% del peso corporal total de una persona, este consume cerca del 20% de la energía de todo el organismo. Dicha demanda metabólica requiere un suministro constante de oxígeno y glucosa. No obstante, el trabajo de las neuronas no es simultáneo en todas las áreas; cuando alguien lee, evoca un recuerdo o realiza un movimiento físico, ciertas regiones se activan con mayor intensidad y precisan un aumento inmediato de irrigación sanguínea.
Durante décadas, la comunidad científica comprendió que los vasos sanguíneos podían experimentar una dilatación (ensanchamiento) para permitir el tránsito de más sangre. Sin embargo, la gran incógnita era cómo ese ajuste en un punto específico afectaba al conjunto de la red. Se desconocía si la modificación del diámetro de un vaso se limitaba a su zona inmediata o si generaba repercusiones en sectores más amplios del sistema.
Para hallar respuestas, el equipo de Kleinfeld y Xiang desarrolló un sofisticado modelo matemático que recrea el comportamiento de la red vascular en su totalidad. Este análisis no se enfoca en un vaso de forma aislada, sino en la arquitectura global del sistema. Utilizando datos reales sobre las conexiones vasculares cerebrales, los expertos pudieron predecir qué ocurre exactamente cuando se altera la estructura de uno de estos conductos.
Una organización precisa tras el aparente caos
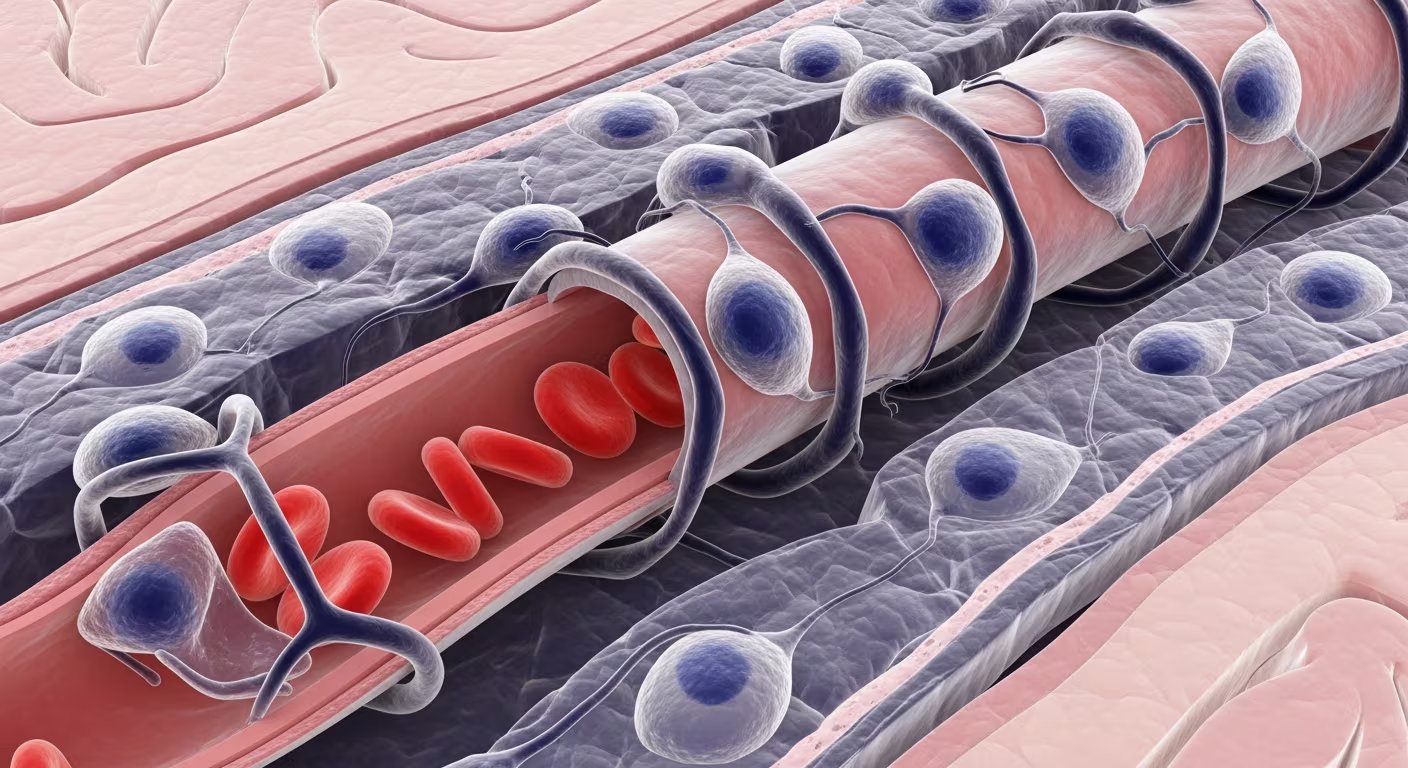
A simple vista, la red de vasos sanguíneos en el cerebro parece un entramado desordenado. Las arterias principales se ramifican en arteriolas, que a su vez se dividen en capilares sumamente finos, por donde los glóbulos rojos circulan prácticamente uno tras otro en fila india.
Para entender este sistema, es útil compararlo con el tráfico en una ciudad. No todas las calles influyen de la misma manera en el movimiento general de los vehículos. Existen avenidas estratégicas que condicionan la circulación de muchas otras vías. Si se interviene una calle secundaria, el impacto global es mínimo; no obstante, si se altera una arteria principal, el efecto se multiplica por toda la red.
El modelo matemático demostró precisamente este principio: no cualquier vaso sanguíneo tiene la capacidad de modificar el flujo general. Solo ciertos segmentos, ubicados en posiciones determinantes dentro de la red, poseen esa facultad de control.
Capilares de transición: los nodos estratégicos
Uno de los descubrimientos fundamentales del estudio fue identificar el rol de los denominados “capilares de transición”. Estos conductos se encuentran situados inmediatamente después de las arteriolas, justo en el punto donde la sangre empieza a distribuirse hacia las áreas más pequeñas del tejido cerebral.
Las predicciones del modelo señalaron que la dilatación de un solo vaso aislado tiene un impacto limitado. Por el contrario, cuando diversos capilares de transición se dilatan de manera coordinada, el cambio en el flujo sanguíneo es contundente, sólido y predecible en toda la extensión de la red vascular.
Para confirmar estas proyecciones teóricas, los investigadores emplearon microscopía confocal de campo de luz, una técnica de imagen avanzada que permite captar con extrema nitidez células y tejidos vivos en diferentes niveles de profundidad.
Gracias a esta tecnología, rastrearon el movimiento de células sanguíneas individuales en la corteza cerebral con una precisión espacial de dos micras y una resolución temporal de apenas catorce milisegundos. En total, el análisis abarcó más de un millón de trayectorias dentro de una red que integraba más de 3.000 ramificaciones interconectadas.
Pericitos: las válvulas biológicas del cerebro
En los puntos de división vascular —las bifurcaciones—, el equipo científico notó la presencia constante de pericitos, células especializadas que rodean los capilares. Estas células tienen la función de influir en el diámetro del vaso, permitiendo su contracción o su relajación según sea necesario.
Su emplazamiento no es casual. Los pericitos se concentran en los nodos divergentes, es decir, donde un vaso se bifurca en varias ramas pequeñas cerca de las arteriolas penetrantes. En esos puntos, funcionan como pequeñas válvulas biológicas que regulan con minuciosidad la distribución de la sangre a microescala.
El estudio también determinó que la estructura vascular demanda coordinación: si solo un tramo varía, el sistema tiende a compensarlo. Pero cuando los puntos estratégicos actúan en conjunto, el efecto se propaga de forma coherente.
Otro dato relevante de la investigación es que el flujo de sangre puede presentar correlaciones, e incluso anticorrelaciones, entre sectores distantes. Esto significa que si la circulación aumenta en una región, puede reducirse en otra para preservar un equilibrio global de recursos.
Adicionalmente, el análisis detallado reveló que en las bifurcaciones puede ocurrir una separación estocástica entre el suero y las células sanguíneas, dependiendo de las condiciones del flujo local, lo cual impacta en cómo se reparten los componentes de la sangre en el tejido.
Trascendencia para la medicina y la ciencia
Entender esta dinámica es crucial para mejorar la interpretación de tecnologías como la resonancia magnética funcional, la cual detecta variaciones en la circulación como un indicador de la actividad de las neuronas. Con un conocimiento más profundo de la redistribución sanguínea, se podrán leer con mayor exactitud las señales de estas imágenes médicas.
Este trabajo también abre nuevas puertas para la investigación de trastornos cerebrovasculares y otras condiciones médicas donde la regulación del flujo sanguíneo se ve alterada o dañada.
En conclusión, lejos de ser un conjunto estático de conductos, la vasculatura del cerebro es un sistema dinámico y altamente coordinado. El flujo no depende de un solo vaso, sino de la interacción entre la arquitectura de la red y la intervención localizada de células especializadas.
Como si se tratara de un sistema de riego automatizado que gestiona compuertas en puntos clave, el cerebro regula su suministro de sangre con una precisión admirable. La investigación de Kleinfeld y Xiang proporciona una pieza esencial para comprender el balance que sostiene cada pensamiento, cada movimiento y cada recuerdo del ser humano.
Fuente: Fuente